氨基酸
氨基酸·
α碳是紧邻羧基的碳,而α碳连接一个氨基,称为α-氨基酸。
水解·
- 完全水解水解为氨基酸
- 不完全水解水解为大小不等的肽和氨基酸
- 水解方法
- 酸水解
不消旋。多数氨基酸稳定,Trp完全破坏,羟基氨基酸部分分解,Gln、Asn酰胺基被水解。
- 碱水解
消旋。多数氨基酸破环,Trp稳定,Arg脱氢。
- 酶水解
不消旋。氨基酸稳定。需多种酶协同。
- 酸水解
分类·
- 是否组成蛋白质
- 稀有蛋白质氨基酸
- 非蛋白质氨基酸
为游离态。
- 蛋白质氨基酸
也称基本/标准/编码氨基酸。20种。都是α-氨基酸。图例
- 碳的命名
以α碳(2号碳)是紧邻羧基(1号碳)的碳,作为起始,往R基上依次排列。
- 碳的命名
- R基团化学结构
- 芳香族AA (3种)
- 杂环AA (2种)
- 脂肪族AA
- 含羟基/巯基 (4种)
- 中性 (5种)
- 酸性 (4种)
- 碱性 (3种)
- R基团极性
- 非极性R基团AA (8种)
- 极性R基团AA
- 不带电荷 (7种)
- 带正电荷 (3种)
- 带负电荷 (2种)
- 营养学
- 必需AA (8种)
- 非必需AA
- 氨基、羧基数目
- 一氨基一羧基AA
- 二氨基一羧基AA
- 一氨基二羧基AA
22种氨基酸·
- 中性脂肪族AA (5种)
- 甘氨酸(Gly,G)

- 丙氨酸(Ala,A)
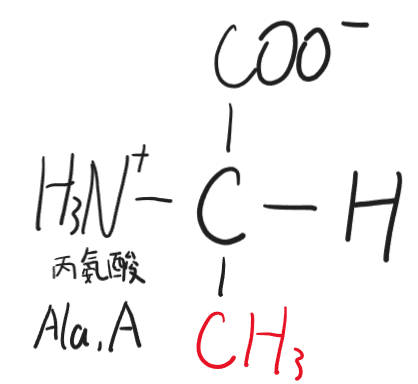
- 缬氨酸(Val,V)
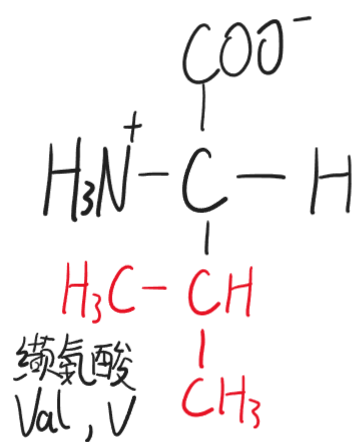
- 亮氨酸(Leu,L)
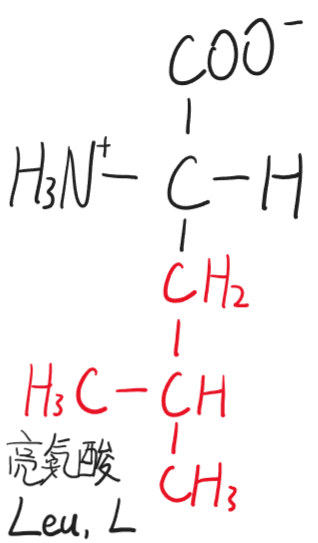
- 异亮氨酸(Ile,I)
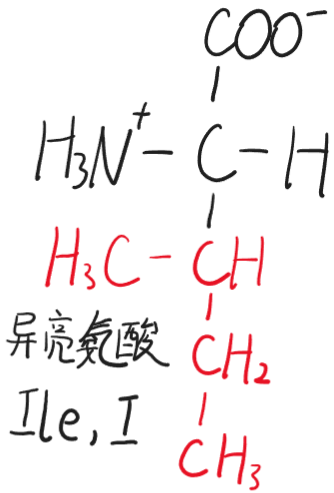
- 甘氨酸(Gly,G)
- 含羟基/巯基脂肪族AA (4种)
- 丝氨酸(Ser,S)
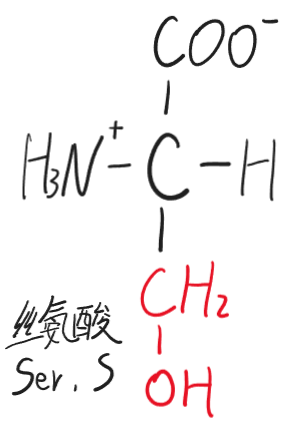
- 苏氨酸(Thr,T)
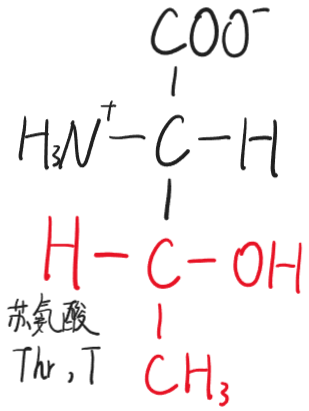
- 半胱氨酸(Cys,C)
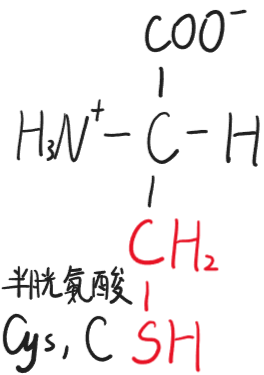
- 甲硫氨酸(Met,M)
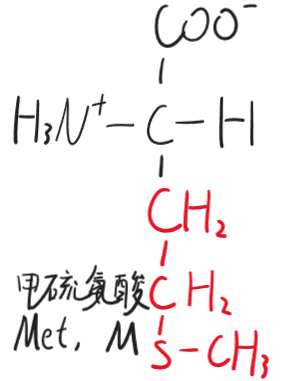
- 丝氨酸(Ser,S)
- 酸性脂肪族AA及酰胺 (4种)
- 天冬氨酸(Asp,D)

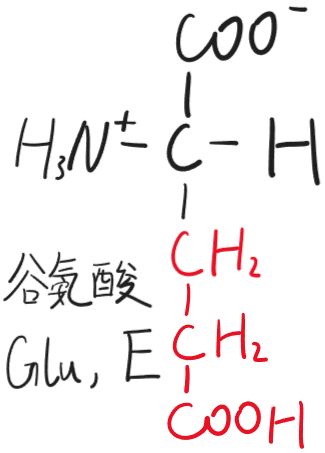
- 谷氨酸(Glu,E)
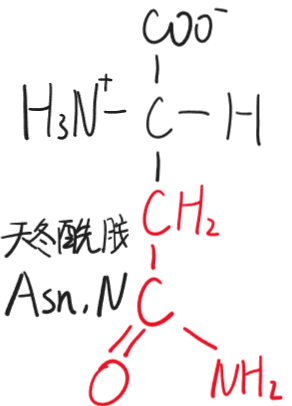
- 天冬酰胺(Asn,N)
- 谷氨酰胺(Gln,Q)

- 天冬氨酸(Asp,D)
- 碱性脂肪族AA (3种)
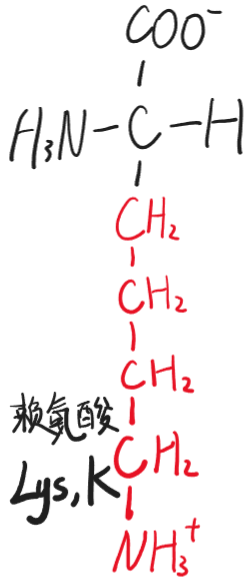
- 赖氨酸(Lys,K)
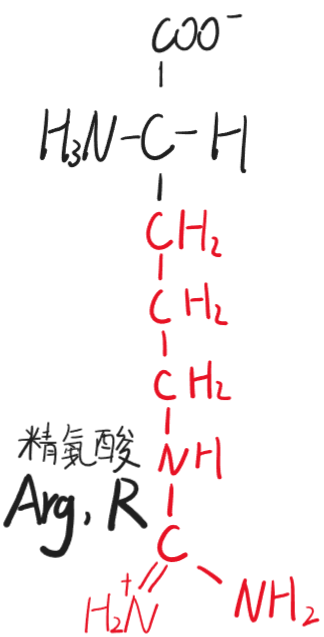
- 精氨酸(Arg,R)
- 组氨酸(His,H)
- 赖氨酸(Lys,K)
- 杂环AA (2种)
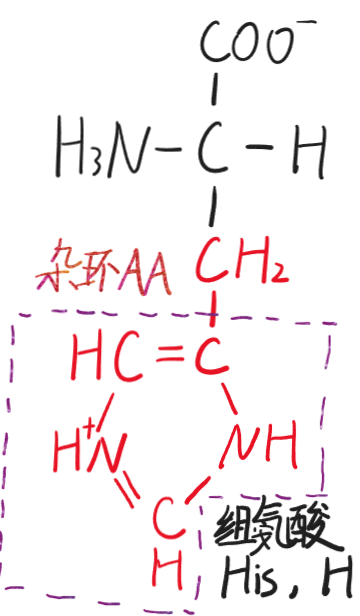
- 组氨酸(His,H)

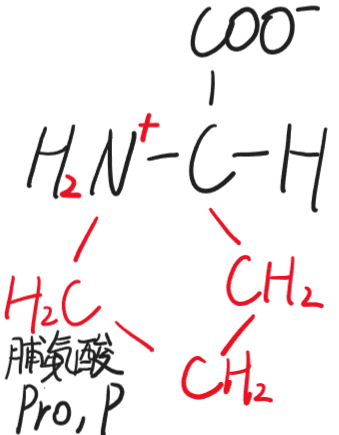
- 脯氨酸(Pro,P)
- 组氨酸(His,H)
- 芳香族AA (3种)
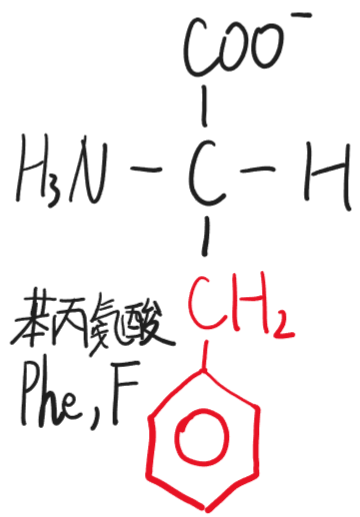
- 苯丙氨酸(Phe,F)
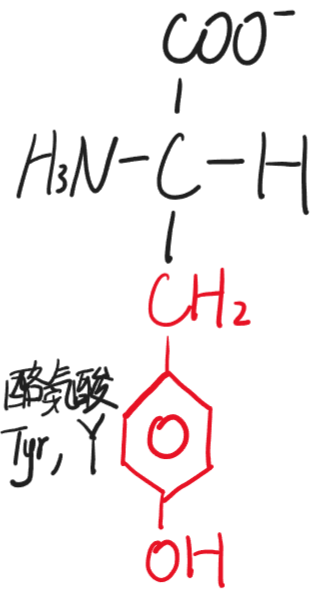
- 酪氨酸(Tyr,Y)
- 色氨酸(Trp,W)
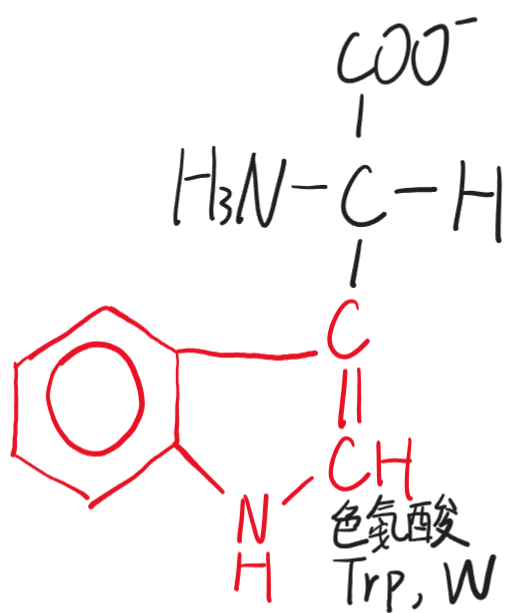
- 苯丙氨酸(Phe,F)
- 其他AA
- 硒代半胱氨酸(Sec) 3-硒基-L-丙氨酸
- 吡咯赖氨酸(Pyl)
性质·
-
物理性质
- 溶解性
溶于水,易溶于稀酸稀碱溶液。不溶于乙醚氯仿等有机溶剂。
- 熔点
均大于200℃。说明氨基酸是以离子态存在,通过离子键结合。
- 旋光性
除了甘氨酸以外均有旋光性。(Thr、Ile等AA有4种光学异构体)
- 紫外吸收光谱
F、Y、W含苯环,在紫外光区显示特征的吸收谱带,Imax为280、275、256nm。
- 溶解性
-
化学性质这里主要讨论酸碱性质。
- 化学反应
- 与α-氨基的反应
- DNFB/FDNB反应
- PITC反应
- 茚三酮反应(羧基也参与)
- 荧光试剂反应
- 与α-羧基的反应
- 酯化反应
- 酰氯化反应
- α-氨基与α-羧基间的成肽键反应
- R基团的反应
- 与α-氨基的反应
- AA的存在形态
大部分氨基酸以兼性离子形式存在。AA兼性离子态
- AA的两性解离性质
- 等电点
pI为等电点,指在一定pH时,氨基酸分子上所带正负电荷相等,使之成为两性离子。
- 两性解离
将氨基酸溶液加碱,氨基上的质子解离。随后加酸,复原。继续加酸,羧基质子化。再后加碱,复原。
pH = pI时,净电荷为0。pH > pI时,氨基酸为净电荷为负。pH < pI时,净电荷为正。
- 等电点
- AA的滴定(以G为例)
Cl-H3N+-CH2-COOH <–> H3N+-CH2-COO- <–> H2N-CH2-COO-Na+
甘氨酸盐酸盐(A+) <–> 等电点甘氨酸(A0) <–> 甘氨酸钠(A-)
Ka1 = [H+][A0]/[A+] Ka2 = [H+][A-]/[A0]
Ka1*Ka2 = [H+]2 * [A-]/[A+]
[H+] = (Ka1*Ka2)1/2
pI = (pKa1+pKa2)/ 2
一氨基二羧基AA:
pI = (pKa1+pKa2) / 2
二氨基一羧基AA:
pI = (pKa2+pKa3) / 2
- 化学反应
考点总结及名词解释·
有待补充
